Mosaïcisme somatique et traçage des lignées
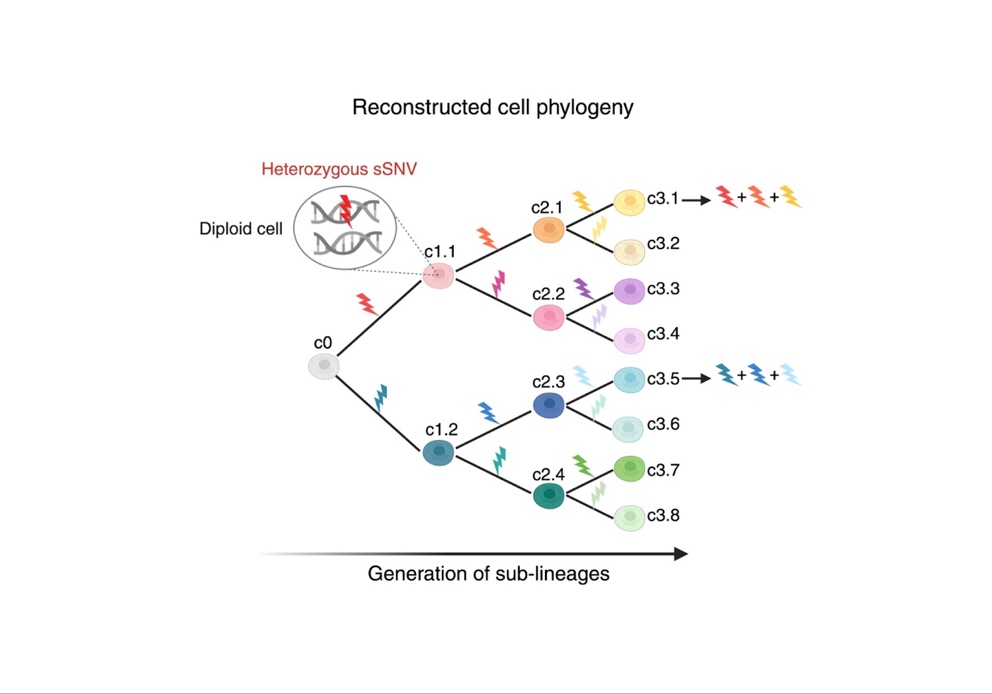 Le développement est un processus concerté de génération de cellules et de spécification de différents types cellulaires. Les cellules progénitrices prolifèrent pour construire les différentes parties du corps, tandis que les tissus et les cellules se différencient à la suite de l'exécution de programmes d'expression génétique précis. La manière dont les cellules sont générées et distribuées dans notre corps est une question clé de la biologie du développement. Les divisions cellulaires successives génèrent des lignées (ou clones) de cellules apparentées qui peuvent être résolues et visualisées sous la forme d'une phylogénie cellulaire dans le cadre d'un processus appelé traçage des lignées. Le traçage des lignées se fait par le marquage permanent, unique et cumulatif des cellules progénitrices, et permet de cartographier et de suivre les cellules au cours du développement. Dans les modèles animaux et in vitro, le traçage de la lignée peut être effectué en introduisant artificiellement des étiquettes (ou cicatrices) dans les cellules progénitrices, par exemple par édition du génome. Chez l'homme, de telles expériences ne peuvent être réalisées in vivo. Toutefois, des études récentes ont montré que les variants nucléotidiques simples somatiques post-zygotiques (sSNV) qui se produisent dans les cellules progénitrices à pratiquement chaque cycle cellulaire et qui n'ont pas d'effet pathologique connu, peuvent être utilisés pour effectuer un traçage rétrospectif de la lignée en partant directement du tissu humain.
Le développement est un processus concerté de génération de cellules et de spécification de différents types cellulaires. Les cellules progénitrices prolifèrent pour construire les différentes parties du corps, tandis que les tissus et les cellules se différencient à la suite de l'exécution de programmes d'expression génétique précis. La manière dont les cellules sont générées et distribuées dans notre corps est une question clé de la biologie du développement. Les divisions cellulaires successives génèrent des lignées (ou clones) de cellules apparentées qui peuvent être résolues et visualisées sous la forme d'une phylogénie cellulaire dans le cadre d'un processus appelé traçage des lignées. Le traçage des lignées se fait par le marquage permanent, unique et cumulatif des cellules progénitrices, et permet de cartographier et de suivre les cellules au cours du développement. Dans les modèles animaux et in vitro, le traçage de la lignée peut être effectué en introduisant artificiellement des étiquettes (ou cicatrices) dans les cellules progénitrices, par exemple par édition du génome. Chez l'homme, de telles expériences ne peuvent être réalisées in vivo. Toutefois, des études récentes ont montré que les variants nucléotidiques simples somatiques post-zygotiques (sSNV) qui se produisent dans les cellules progénitrices à pratiquement chaque cycle cellulaire et qui n'ont pas d'effet pathologique connu, peuvent être utilisés pour effectuer un traçage rétrospectif de la lignée en partant directement du tissu humain.
Lignées cellulaires du développement neurologique humain
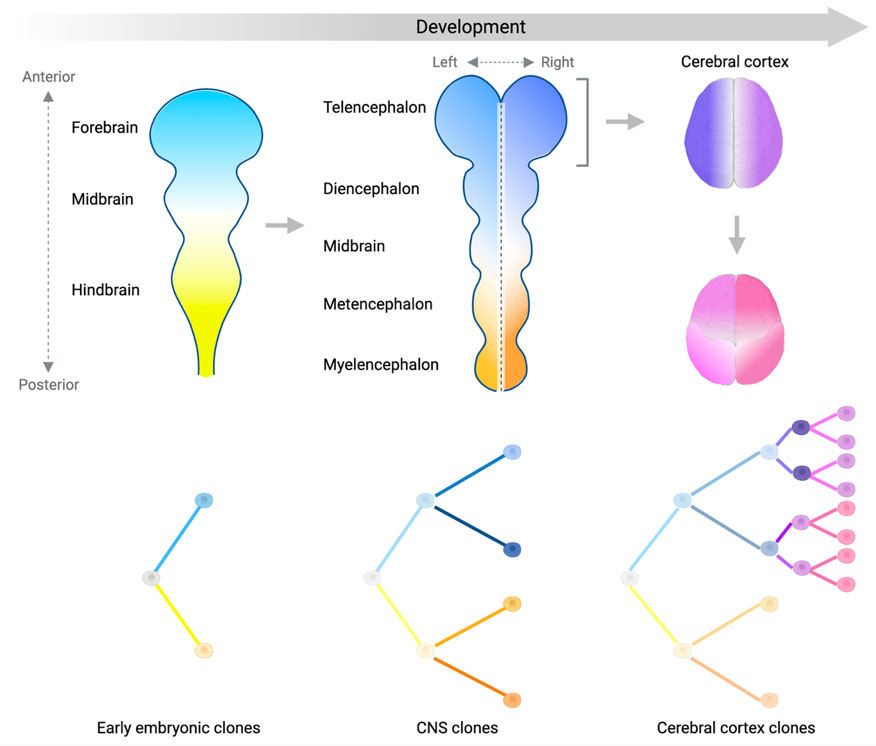
Le système nerveux central humain (SNC) est une mosaïque de plus de 200 milliards de cellules. Le développement du SNC commence par la formation du tube neural après la gastrulation et se termine par la structure cérébrale la plus évoluée et la plus complexe, le cortex cérébral. La manière dont les cellules façonnent le SNC au cours du développement est une question qui se pose depuis longtemps en neurobiologie. Les caractéristiques structurelles propres à l'homme ne sont que partiellement récapitulées dans les modèles existants, ce qui rend d'autant plus nécessaire la réalisation d'études directement chez l'homme. L'un des objectifs de notre laboratoire est de cartographier et de retracer l'origine développementale des cellules du SNC humain afin de comprendre sa formation. Pour ce faire, nous utilisons des tissus humains post-mortem et appliquons des technologies de séquençage de pointe, notamment le séquençage de l'ADN en vrac et unicellulaire, ainsi que des techniques (multi)omiques unicellulaires. Notre laboratoire utilise également des outils informatiques avancés et la modélisation mathématique pour répondre à ces questions et interpréter les processus stochastiques et déterministes agissant sur les lignées cellulaires et l'évolution somatique.
Troubles cérébraux pédiatriques
Les troubles cérébraux pédiatriques comprennent les troubles du développement neurologique tels que les malformations corticales, ainsi que les tumeurs cérébrales de bas et de haut grade. Les malformations corticales constituent un large éventail de troubles rares du développement du cerveau, d'origine génétique, souvent non syndromiques, associés à une épilepsie pharmaco-résistante. Bien que les causes génétiques de certains de ces troubles soient connues, une fraction importante des cas (~45%) n'est toujours pas résolue sur le plan génétique. Les tumeurs cérébrales pédiatriques, quant à elles, comprennent les tumeurs associées à l'épilepsie de bas grade (LEAT) telles que le gangliogliome (GG), les tumeurs neuroépithéliales dysembryoplastiques (DNT) et l'astrocytome pilocytique, et les tumeurs de haut grade telles que le gliome pontin intrinsèque diffus de l'enfant (DIPG), la tumeur rhabdoïde tératoïde atypique (ATRT) et les tumeurs cérébrales embryonnaires telles que le médulloblastome de l'enfant. Notre laboratoire s'efforce 1) d'étudier le rôle potentiel des variantes somatiques dans certains de ces troubles ; 2) de caractériser le paysage génomique somatique des tumeurs cérébrales pédiatriques, et 3) de comprendre l'origine des troubles et leur développement somatique en mettant l'accent sur les lignées cellulaires.